par admin | Juil 10, 2024 | Santé
En un coup d’oeil
- L’étude de preuve de concept représente la première tentative réussie d’inverser l’horloge du vieillissement chez les animaux grâce à la reprogrammation épigénétique.
- Les scientifiques ont activé des gènes embryonnaires pour reprogrammer les cellules de la rétine de souris.
- L’approche a inversé les lésions oculaires induites par le glaucome chez les animaux.
- L’approche a également restauré la perte de vision liée à l’âge chez les souris âgées.
- Les sorts de travail promettent d’utiliser la même approche dans d’autres tissus, organes au-delà des yeux.
- Le succès ouvre la voie au traitement de diverses maladies liées à l’âge chez l’homme.
Harvard Medical School
Des scientifiques de la Harvard Medical School ont réussi à restaurer la vision chez la souris en remontant le temps sur les cellules oculaires âgées de la rétine pour retrouver la fonction des gènes jeunes.
Le travail de l’équipe, décrit le 2 décembre dans Nature, représente la première démonstration qu’il peut être possible de reprogrammer en toute sécurité des tissus complexes, tels que les cellules nerveuses de l’œil, à un âge plus précoce.
En plus de réinitialiser l’horloge de vieillissement des cellules, les chercheurs ont réussi à inverser la perte de vision chez les animaux atteints d’une maladie imitant le glaucome humain, l’une des principales causes de cécité dans le monde.
Cette réalisation représente la première tentative réussie d’inverser la perte de vision induite par le glaucome, plutôt que de simplement endiguer sa progression, a déclaré l’équipe.
Si elle est reproduite par d’autres études, l’approche pourrait ouvrir la voie à des thérapies visant à promouvoir la réparation des tissus dans divers organes et à inverser le vieillissement et les maladies liées à l’âge chez l’homme.

David Sinclair, PhD, et Yuancheng Lu, PhD
« Notre étude démontre qu’il est possible d’inverser en toute sécurité l’âge de tissus complexes tels que la rétine et de restaurer sa fonction biologique juvénile », a déclaré l’auteur principal David Sinclair, PhD, professeur de génétique à l’Institut Blavatnik de la Harvard Medical School, co-directeur du Paul F. Glenn Center for Biology of Aging Research à HMS et expert du vieillissement.
Sinclair et ses collègues préviennent que les résultats doivent encore être reproduits dans d’autres études, y compris dans différents modèles animaux, avant toute expérience humaine. Néanmoins, ajoutent-ils, les résultats offrent une preuve de concept et une voie vers la conception de traitements pour une gamme de maladies humaines liées à l’âge.
« S’ils sont confirmés par d’autres études, ces résultats pourraient transformer le traitement des maladies de la vision liées à l’âge comme le glaucome et les domaines de la biologie et de la thérapeutique médicale pour la maladie en général », a déclaré Sinclair.
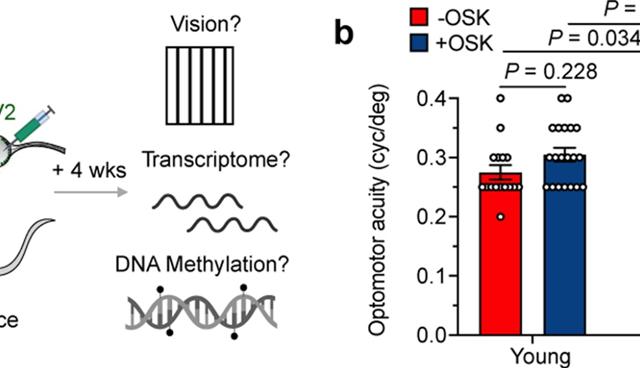
Pour leur travail, l’équipe a utilisé un virus adéno-associé (AAV) comme véhicule pour délivrer dans la rétine de souris trois gènes de restauration de la jeunesse – Oct4, Sox2 et Klf4 – qui sont normalement activés pendant le développement embryonnaire. Les trois gènes, ainsi qu’un quatrième, qui n’a pas été utilisé dans ce travail, sont collectivement connus sous le nom de facteurs Yamanaka.
Le traitement a eu de multiples effets bénéfiques sur l’œil. Premièrement, il a favorisé la régénération nerveuse après une lésion du nerf optique chez les souris dont les nerfs optiques étaient endommagés. Deuxièmement, il a inversé la perte de vision chez les animaux atteints d’une maladie imitant le glaucome humain. Et troisièmement, il a inversé la perte de vision chez les animaux vieillissants sans glaucome.
L’approche de l’équipe est basée sur une nouvelle théorie sur les raisons pour lesquelles nous vieillissons. La plupart des cellules du corps contiennent les mêmes molécules d’ADN mais ont des fonctions très diverses. Pour atteindre ce degré de spécialisation, ces cellules ne doivent lire que les gènes spécifiques à leur type. Cette fonction régulatrice est du ressort de l’épigénome, un système d’activation et de désactivation des gènes selon des schémas spécifiques sans altérer la séquence d’ADN sous-jacente de base du gène.
Cette théorie postule que les changements apportés à l’épigénome au fil du temps amènent les cellules à lire les mauvais gènes et à mal fonctionner, ce qui donne lieu à des maladies liées au vieillissement. L’un des changements les plus importants de l’épigénome est la méthylation de l’ADN, un processus par lequel des groupes méthyles sont ajoutés à l’ADN. Des modèles de méthylation de l’ADN sont établis au cours du développement embryonnaire pour produire les différents types de cellules. Au fil du temps, les modèles de méthylation de l’ADN sont perdus et les gènes à l’intérieur des cellules qui devraient être activés sont désactivés et vice versa, ce qui entraîne une altération de la fonction cellulaire. Certains de ces changements de méthylation de l’ADN sont prévisibles et ont été utilisés pour déterminer l’âge biologique d’une cellule ou d’un tissu.
Pourtant, on ne sait pas si la méthylation de l’ADN entraîne des changements liés à l’âge à l’intérieur des cellules. Dans la présente étude, les chercheurs ont émis l’hypothèse que si la méthylation de l’ADN contrôle effectivement le vieillissement, l’effacement de certaines de ses empreintes pourrait inverser l’âge des cellules à l’intérieur des organismes vivants et les restaurer à leur état antérieur et plus jeune. Des travaux antérieurs avaient réalisé cet exploit dans des cellules cultivées dans des boîtes de laboratoire, mais n’avaient pas réussi à démontrer l’effet sur les organismes vivants.
Les nouvelles découvertes démontrent que l’approche pourrait également être utilisée chez les animaux.
Surmonter un obstacle important
Auteur principal de l’étude,Yuancheng Lu, Ph. D.,chercheur en génétique à HMS et ancien doctorant dans le laboratoire de Sinclair, a mis au point une thérapie génique qui pourrait inverser en toute sécurité l’âge des cellules d’un animal vivant.
Le travail de Lu s’appuie sur la découverte de Shinya Yamanaka, lauréat du prix Nobel, qui a identifié les quatre facteurs de transcription, Oct4, Sox2, Klf4, c-Myc, qui pourraient effacer les marqueurs épigénétiques sur les cellules et ramener ces cellules à leur état embryonnaire primitif à partir duquel elles peuvent se développer en tout autre type de cellule.
Des études ultérieures, cependant, ont montré deux revers importants. Tout d’abord, lorsqu’ils sont utilisés chez des souris adultes, les quatre facteurs Yamanaka pourraient également induire la croissance tumorale, rendant l’approche dangereuse. Deuxièmement, les facteurs pourraient réinitialiser l’état cellulaire à l’état cellulaire le plus primitif, effaçant ainsi complètement l’identité d’une cellule.
Lu et ses collègues ont contourné ces obstacles en modifiant légèrement l’approche. Ils ont abandonné le gène c-Myc et n’ont livré que les trois gènes Yamanaka restants, Oct4, Sox2 et Klf4. L’approche modifiée a réussi à inverser le vieillissement cellulaire sans alimenter la croissance tumorale ni perdre leur identité.
Thérapie génique appliquée à la régénération du nerf optique
Dans la présente étude, les chercheurs ont ciblé les cellules du système nerveux central car il s’agit de la première partie du corps affectée par le vieillissement. Après la naissance, la capacité du système nerveux central à se régénérer diminue rapidement.
Pour tester si la capacité de régénération des jeunes animaux pouvait être transmise à des souris adultes, les chercheurs ont délivré la combinaison modifiée de trois gènes via un AAV dans les cellules ganglionnaires rétiniennes de souris adultes atteintes de lésions du nerf optique.

Fig. 2 : Régénération des axones après l’écrasement du nerf optique chez les souris âgées ayant reçu un traitement OSK
Pour ce travail, Lu et Sinclair se sont associés à Zhigang He, PhD, professeur de neurologie et d’ophtalmologie HMS à l’hôpital pour enfants de Boston, qui étudie la neuro-régénération du nerf optique et de la moelle épinière.
Le traitement a entraîné une multiplication par deux du nombre de cellules ganglionnaires rétiniennes survivantes après la blessure et une multiplication par cinq de la repousse nerveuse.
« Au début de ce projet, beaucoup de nos collègues ont dit que notre approche échouerait ou serait trop dangereuse pour être utilisée », a déclaré Lu. « Nos résultats suggèrent que cette méthode est sûre et pourrait potentiellement révolutionner le traitement de l’œil et de nombreux autres organes affectés par le vieillissement. »
Inversion du glaucome et de la perte de vision liée à l’âge
Suite aux résultats encourageants chez les souris souffrant de lésions du nerf optique, l’équipe s’est associée à des collègues du Schepens Eye Research Institute of Massachusetts Eye and Ear Bruce Ksander, PhD, professeur agrégé d’ophtalmologie HMS, et Meredith Gregory-Ksander, PhD, professeur adjoint d’ophtalmologie HMS. Ils ont planifié deux séries d’expériences : une pour tester si le cocktail de trois gènes pouvait restaurer la perte de vision due au glaucome et une autre pour voir si l’approche pouvait inverser la perte de vision résultant du vieillissement normal.

Fig. 3 : Bruce Ksander, Ph. D., et Meredith Gregory-Ksander, Ph. D.
Dans un modèle murin de glaucome, le traitement a entraîné une augmentation de l’activité électrique des cellules nerveuses et une augmentation notable de l’acuité visuelle, mesurée par la capacité des animaux à voir des lignes verticales en mouvement sur un écran. Remarquablement, il l’a fait après que la perte de vision induite par le glaucome se soit déjà produite.
« Retrouver la fonction visuelle après la blessure a rarement été démontré par les scientifiques », a déclaré Ksander. « Cette nouvelle approche, qui inverse avec succès de multiples causes de perte de vision chez la souris sans avoir besoin d’une greffe de rétine, représente une nouvelle modalité de traitement en médecine régénérative. »
Le traitement a également fonctionné chez les souris âgées de 12 mois dont la vision diminue en raison du vieillissement normal. Après le traitement des souris âgées, les modèles d’expression génique et les signaux électriques des cellules du nerf optique étaient similaires à ceux des jeunes souris, et la vision a été restaurée.
Lorsque les chercheurs ont analysé les changements moléculaires dans les cellules traitées, ils ont trouvé des schémas inversés de méthylation de l’ADN – une observation suggérant que la méthylation de l’ADN n’est pas un simple marqueur ou un spectateur dans le processus de vieillissement, mais plutôt un agent actif qui le conduit.
« Ce que cela nous dit, c’est que l’horloge ne représente pas seulement le temps, c’est le temps », a déclaré Sinclair. « Si vous remontez les aiguilles de l’horloge, le temps recule également. »
« Actuellement, les stratégies de traitement de nombreuses maladies oculaires liées à l’âge, comme le glaucome, sont axées sur le ralentissement de la progression de la maladie et la préservation de la vision restante du patient. Cette recherche est très prometteuse, car elle pourrait finalement conduire à une nouvelle classe de traitements qui pourraient restaurer une vision déjà perdue », a déclaré Joan W. Miller, MD, chef de l’ophtalmologie au Mass Eye and Ear, Massachusetts General Hospital, et ophtalmologiste en chef au Brigham and Women’s Hospital, et président de l’ophtalmologie et professeur David Glendenning Cogan d’ophtalmologie à la Harvard Medical School.
Les chercheurs ont déclaré que si leurs résultats sont confirmés par d’autres travaux sur les animaux, ils pourraient lancer des essais cliniques dans les deux ans pour tester l’efficacité de l’approche chez les personnes atteintes de glaucome. Jusqu’à présent, les résultats sont encourageants, ont déclaré les chercheurs. Dans la présente étude, un traitement d’un an sur l’ensemble du corps de souris avec l’approche à trois gènes n’a montré aucun effet secondaire négatif.
Parmi les autres auteurs de l’article figurent Benedikt Brommer, Xiao Tian, Anitha Krishnan, Margarita Meer, Chen Wang, Daniel Vera, Qiurui Zeng, Doudou Yu, Michael Bonkowski, Jae-Hyun Yang, Songlin Zhou, Emma Hoffmann, Margarete Karg, Michael Schultz, Alice Kane, Noah Davidsohn, Ekaterina Korobkina, Karolina Chwalek, Luis Rajman, George Church, Konrad Hochedlinger, Vadim Gladyshev, Steve Horvath et Morgan Levine.
Ce travail a été soutenu en partie par une subvention de démarrage et de développement de l’épigénétique de la Harvard Medical School, la Fondation Glenn pour la recherche médicale, Edward Schulak, les National Institutes of Health et la Fondation Saint-Vincent-de-Paul.
Divulgations pertinentes : David Sinclair est consultant, inventeur de brevets concédés sous licence, membre du conseil d’administration et actionnaire d’Iduna Therapeutics, une société de biosciences de la vie qui développe des thérapies de reprogrammation épigénétique, et consultant non rémunéré de Zymo Research, une société d’outils épigénétiques. Yuancheng Lu, Luis Rajman et Steve Horvath sont actionnaires d’Iduna Therapeutics. George Church et Noah Davidsohn sont les cofondateurs de Rejuvenate Bio. D’autres divulgations de Sinclair et de Church sont à http://arep.med.harvard.edu/gmc/tech.html et https://genetics.med.harvard.edu/sinclair/people/sinclair-other.php.
À propos de la Harvard Medical School
La Harvard Medical School compte plus de 11 000 professeurs travaillant dans les 11 départements de sciences fondamentales et sociales composant l’Institut Blavatnik et dans les 15 hôpitaux universitaires et instituts de recherche affiliés à Harvard : Beth Israel Deaconess Medical Center, Boston Children’s Hospital, Brigham and Women’s Hospital, Cambridge Health Alliance, Dana-Farber Cancer Institute, Harvard Pilgrim Health Care Institute, Hebrew SeniorLife, Joslin Diabetes Center, Judge Baker Children’s Center, Massachusetts Eye and Ear/Schepens Eye Research Institute, Massachusetts General Hospital, McLean Hospital, Mount Auburn Hospital, Spaulding Rehabilitation Network et VA Boston Healthcare System.
À propos de Mass Eye and Ear
Massachusetts Eye and Ear, fondé en 1824, est un centre international de traitement et de recherche et un hôpital universitaire de la Harvard Medical School. Membre de Mass General Brigham, Mass Eye and Ear se spécialise en ophtalmologie (soins oculaires) et en oto-rhino-laryngologie – chirurgie de la tête et du cou (soins des oreilles, du nez et de la gorge). Les cliniciens de Mass Eye and Ear fournissent des soins allant de la routine au très complexe. Abritant également la plus grande communauté de chercheurs en audition et en vision au monde, les scientifiques de Mass Eye and Ear ont pour mission de découvrir la biologie de base des affections sous-jacentes affectant les yeux, les oreilles, le nez, la gorge, la tête et le cou et de développer de nouveaux traitements et remèdes. Dans l’enquête 2020-2021 sur les meilleurs hôpitaux, U.S. News & World Report a classé Mass Eye and Ear #4 dans le pays pour les soins oculaires et #6 pour les soins des oreilles, du nez et de la gorge. Pour plus d’informations sur les soins et la recherche qui changent la vie à Mass Eye and Ear, visitez notre blog, Focus, et suivez-nous sur Instagram, Twitter et Facebook.
À propos du département d’ophtalmologie de la Harvard Medical School
Le département d’ophtalmologie de la Harvard Medical School est l’un des principaux et des plus grands départements universitaires d’ophtalmologie du pays. Composé de neuf affiliés (Massachusetts Eye and Ear, qui abrite le Schepens Eye Research Institute ; Hôpital général du Massachusetts ; Hôpital Brigham and Women’s ; Hôpital pour enfants de Boston ; Centre médical Beth Israel Deaconess ; Centre du diabète Joslin/Institut ophtalmologique Beetham ; le système de santé des anciens combattants de Boston ; le système de santé des anciens combattants du Maine ; et Cambridge Health Alliance) et plusieurs partenaires internationaux, le département s’appuie sur les ressources d’une équipe mondiale pour poursuivre un objectif unique : éradiquer les maladies cécitantes afin que tous les enfants nés aujourd’hui puissent les voir tout au long de leur vie. Officiellement créé en 1871, le département s’engage à remplir sa triple mission : fournir des soins cliniques de premier ordre, mener des recherches transformationnelles et offrir une formation de classe mondiale aux leaders de demain en ophtalmologie.
NATURE, 588,124-129 (2020)
Reprogramming to recover youthful epigenetic information and restore vision
Yuancheng Lu, Benedikt Brommer, Xiao Tian, Anitha Krishnan, Margarita Meer, Chen Wang, Daniel L. Vera, Qiurui Zeng, Doudou Yu, Michael S. Bonkowski, Jae-Hyun Yang, Songlin Zhou, Emma M. Hoffmann, Margarete M. Karg, Michael B. Schultz, Alice E. Kane, Noah Davidsohn, Ekaterina Korobkina, Karolina Chwalek, Luis A. Rajman, George M. Church, Konrad Hochedlinger, Vadim N. Gladyshev, Steve Horvath, Morgan E. Levine, Meredith S. Gregory-Ksander, Bruce R. Ksander, Zhigang He & David A. Sinclair
par admin | Juil 10, 2024 | Microbiote, Santé
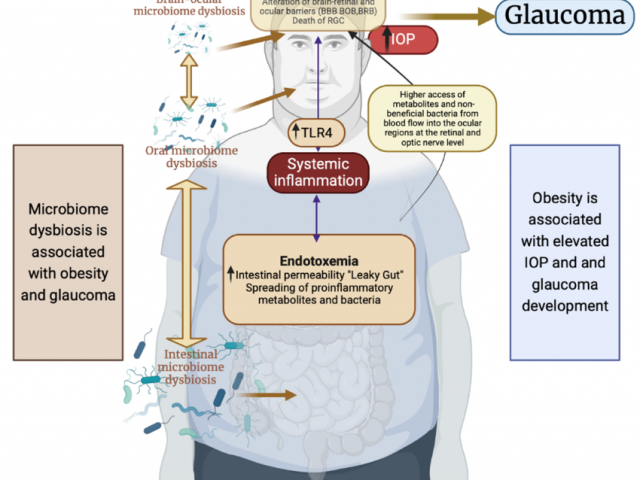
Le lien entre le microbiote et le glaucome
Le microbiote, souvent appelé notre « deuxième cerveau », est un ensemble complexe de micro-organismes vivant dans notre corps, principalement dans notre intestin. Ces milliards de bactéries, virus et autres microbes jouent un rôle crucial dans notre santé globale. Récemment, les scientifiques ont commencé à explorer des liens fascinants entre le microbiote et diverses maladies, y compris le glaucome, une maladie oculaire grave qui peut entraîner la cécité. Dans cet article, nous allons explorer comment le microbiote pourrait influencer le développement et la progression du glaucome.
Qu’est-ce que le glaucome?
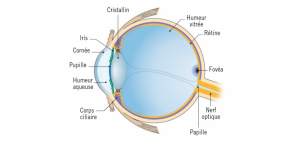 Le glaucome est une maladie oculaire caractérisée par des dommages progressifs au nerf optique, souvent associés à une pression intraoculaire élevée. Il existe plusieurs types de glaucome, mais le plus courant est le glaucome à angle ouvert. Si elle n’est pas traitée, cette condition peut entraîner une perte de vision irréversible.
Le glaucome est une maladie oculaire caractérisée par des dommages progressifs au nerf optique, souvent associés à une pression intraoculaire élevée. Il existe plusieurs types de glaucome, mais le plus courant est le glaucome à angle ouvert. Si elle n’est pas traitée, cette condition peut entraîner une perte de vision irréversible.
Le microbiote intestinal et la santé oculaire
Le microbiote intestinal joue un rôle clé dans le maintien de notre santé en régulant le système immunitaire, en aidant à la digestion et en produisant des vitamines essentielles. Mais comment ces micro-organismes peuvent-ils influencer la santé de nos yeux? Les recherches suggèrent que le microbiote pourrait affecter les voies inflammatoires et immunitaires dans le corps, y compris celles qui touchent les yeux.
Les études récentes
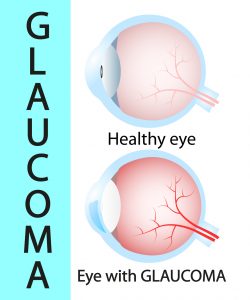
Des études récentes ont commencé à établir des liens entre le microbiote intestinal et le glaucome. Par exemple, des chercheurs ont découvert que les patients atteints de glaucome ont souvent un microbiote intestinal différent de celui des personnes en bonne santé. Ces différences peuvent influencer la manière dont le système immunitaire réagit aux dommages du nerf optique.
Certains déséquilibres dans le microbiote intestinal pourraient être associés à une inflammation systémique accrue, ce qui pourrait exacerber les dommages au nerf optique chez les patients atteints de glaucome. De plus, des essais sur des modèles animaux ont montré que la modification du microbiote intestinal par des probiotiques ou des régimes alimentaires spécifiques pourrait potentiellement réduire la progression du glaucome.

Une étude intéressante sur le lien entre le microbiote intestinal et le glaucome publiée dans la revue « Investigative Ophthalmology & Visual Science ». L’étude, menée par Shida Chen et ses collègues du Centre ophtalmique Zhongshan à Guangzhou, en Chine, étudie la composition du microbiote intestinal et les changements métabolomiques associés chez les patients atteints de glaucome primaire à angle ouvert.
Les chercheurs ont prélevé des échantillons de matières fécales et de sang de 50 patients atteints de glaucome et de 50 témoins sains. L’étude a révélé que les patients atteints de glaucome avaient une diversité de microbiote intestinal inférieure à celle des témoins sains. Plus précisément, ils ont observé une augmentation de Fusobacteriia et une diminution de Clostridia et de Bacilles, y compris des niveaux plus faibles de Ruminococcaceae et de Pasteurellaceae. De plus, l’analyse métabolomique a révélé des niveaux plus élevés d’acides gras à chaîne courte dans les échantillons fécaux et sanguins de patients atteints de glaucome (ARVO Journals).
Cette recherche met en évidence le rôle potentiel du microbiote intestinal dans la pathogenèse du glaucome et suggère que des altérations du microbiote intestinal et de leurs métabolites pourraient être liées au développement et à la progression de cette maladie oculaire.
Pour plus d’informations, vous pouvez vous référer à l’étude intitulée « Microbiote intestinal et changement métabolomique associé dans le glaucome primaire à angle ouvert », publiée dans le numéro de juin 2020 de la revue (ARVO Journals).
Le rôle des probiotiques
Les probiotiques, qui sont des suppléments contenant des bactéries bénéfiques, pourraient jouer un rôle dans la gestion du glaucome. Bien que la recherche soit encore préliminaire, certains essais cliniques suggèrent que les probiotiques pourraient aider à rétablir un équilibre sain du microbiote, réduisant ainsi l’inflammation et peut-être même la pression intraoculaire.
Vers un avenir prometteur
Bien que le lien entre le microbiote et le glaucome soit encore un domaine de recherche émergent, les résultats initiaux sont prometteurs. Comprendre comment les bactéries intestinales influencent notre santé oculaire pourrait ouvrir de nouvelles avenues pour la prévention et le traitement du glaucome. À mesure que la recherche progresse, il est possible que des thérapies basées sur la modulation du microbiote deviennent une partie intégrante de la gestion du glaucome.
Conclusion
Le microbiote intestinal est un acteur crucial de notre santé globale, et son influence s’étend peut-être jusqu’à nos yeux. Les découvertes récentes sur le lien entre le microbiote et le glaucome offrent de nouvelles perspectives passionnantes pour la compréhension et le traitement de cette maladie oculaire dévastatrice. Il est essentiel de continuer à soutenir et à suivre cette recherche pour développer des approches innovantes et efficaces pour protéger notre vision.
Pour en savoir plus sur le lien probable entre le glaucome et le microbiote intestinal ….
The ocular microbiome and microbiota and their effects on ocular surface pathophysiology and disorders.
Aragona P, Baudouin C, Benitez Del Castillo JM, Messmer E, Barabino S, Merayo-Lloves J, Brignole-Baudouin F, Inferrera L, Rolando M, Mencucci R, Rescigno M, Bonini S, Labetoulle M.Surv Ophthalmol. 2021 Nov-Dec;66(6):907-925. doi: 10.1016/j.survophthal.2021.03.010. Epub 2021 Apr 2.
Current Evidence on the Ocular Surface Microbiota and Related Diseases.
Petrillo F, Pignataro D, Lavano MA, Santella B, Folliero V, Zannella C, Astarita C, Gagliano C, Franci G, Avitabile T, Galdiero M.Microorganisms. 2020 Jul 13;8(7):1033. doi: 10.3390/microorganisms8071033.
The Ocular Microbiome: Molecular Characterisation of a Unique and Low Microbial Environment.
Ozkan J, Willcox MD.Curr Eye Res. 2019 Jul;44(7):685-694. doi: 10.1080/02713683.2019.1570526. Epub 2019 Feb 4.
The microbiome and ophthalmic disease.
Baim AD, Movahedan A, Farooq AV, Skondra D.Exp Biol Med (Maywood). 2019 Apr;244(6):419-429. doi: 10.1177/1535370218813616. Epub 2018 Nov 21.
Characterization of the normal microbiota of the ocular surface.
Willcox MD.Exp Eye Res. 2013 Dec;117:99-105. doi: 10.1016/j.exer.2013.06.003. Epub 2013 Jun 22

par admin | Juil 10, 2024 | Santé
 L’huile d’olive, un pilier de la cuisine méditerranéenne, est bien connue pour ses nombreux bienfaits pour la santé, notamment ses effets anti-inflammatoires et cardioprotecteurs. Cependant, une facette moins explorée de cette huile précieuse est son influence sur le microbiote intestinal. Dans cet article, nous allons plonger dans les effets de l’huile d’olive sur notre microbiote et comprendre pourquoi cette alliance est bénéfique pour notre santé globale.
L’huile d’olive, un pilier de la cuisine méditerranéenne, est bien connue pour ses nombreux bienfaits pour la santé, notamment ses effets anti-inflammatoires et cardioprotecteurs. Cependant, une facette moins explorée de cette huile précieuse est son influence sur le microbiote intestinal. Dans cet article, nous allons plonger dans les effets de l’huile d’olive sur notre microbiote et comprendre pourquoi cette alliance est bénéfique pour notre santé globale.
Qu’est-ce que le Microbiote Intestinal ?
Le microbiote intestinal désigne l’ensemble des micro-organismes qui résident dans notre tractus gastro-intestinal. Ce vaste écosystème, composé de bactéries, virus, champignons et autres microbes, joue un rôle crucial dans la digestion, la synthèse de vitamines, la protection contre les pathogènes et la modulation de notre système immunitaire.
Comment l’Huile d’Olive Influence le Microbiote
 1. Effet Prébiotique : Les polyphénols de l’huile d’olive peuvent agir comme des prébiotiques, c’est-à-dire qu’ils favorisent la croissance des bactéries bénéfiques dans l’intestin. Ces composés sont métabolisés par les bactéries intestinales, produisant ainsi des métabolites bénéfiques comme les acides gras à chaîne courte (AGCC), qui sont essentiels pour la santé intestinale et globale.
1. Effet Prébiotique : Les polyphénols de l’huile d’olive peuvent agir comme des prébiotiques, c’est-à-dire qu’ils favorisent la croissance des bactéries bénéfiques dans l’intestin. Ces composés sont métabolisés par les bactéries intestinales, produisant ainsi des métabolites bénéfiques comme les acides gras à chaîne courte (AGCC), qui sont essentiels pour la santé intestinale et globale.
2. Réduction des Inflammations : Les propriétés anti-inflammatoires de l’huile d’olive peuvent aider à réduire l’inflammation intestinale. Une inflammation chronique peut perturber l’équilibre du microbiote, favorisant la croissance de bactéries pathogènes au détriment des bactéries bénéfiques. En réduisant l’inflammation, l’huile d’olive contribue à maintenir un microbiote équilibré et sain.
3. Modulation de la Diversité Microbienne : La consommation régulière d’huile d’olive peut augmenter la diversité microbienne intestinale, un indicateur clé d’un microbiote sain. Une plus grande diversité microbienne est associée à une meilleure santé métabolique et immunitaire.
Études et Recherches
Des études récentes ont montré que les personnes suivant un régime riche en huile d’olive présentent une composition microbienne plus favorable par rapport à celles consommant d’autres types de graisses. Par exemple, une étude publiée dans le Journal of Nutritional Biochemistry a révélé que les polyphénols de l’huile d’olive augmentaient les niveaux de Lactobacillus et de Bifidobacterium, deux genres bactériens bénéfiques.
Une huile sicilienne, produite par Sergio Caseli, s’est revélé être très riche en polyphénols :
Olio Iolanda
https://www.olio-iolanda.com
Conseils pour Intégrer l’Huile d’Olive dans Votre Régime
 1. Utilisation Quotidienne : Utilisez l’huile d’olive comme principal corps gras pour la cuisson et l’assaisonnement. Elle est idéale pour les salades, les légumes rôtis et les marinades.
1. Utilisation Quotidienne : Utilisez l’huile d’olive comme principal corps gras pour la cuisson et l’assaisonnement. Elle est idéale pour les salades, les légumes rôtis et les marinades.
2. Consommation Modérée : Bien que bénéfique, il est important de consommer l’huile d’olive avec modération en raison de sa densité calorique élevée.
3. Choix de Qualité : Optez pour de l’huile d’olive extra vierge de bonne qualité, de préférence pressée à froid, pour maximiser les bénéfices pour le microbiote.
Conclusion
L’huile d’olive ne se contente pas de rehausser la saveur de nos plats ; elle joue également un rôle crucial dans le maintien de notre santé intestinale. En favorisant un microbiote équilibré et diversifié, cette huile précieuse contribue à notre bien-être général. Intégrer l’huile d’olive dans votre alimentation quotidienne est une étape simple mais efficace pour soutenir votre microbiote et, par extension, votre santé globale.
par admin | Juil 10, 2024 | Microbiote, Santé
Le microbiote, cet ensemble complexe de micro-organismes résidant dans notre intestin, est un acteur clé de notre santé. Au cours des dernières décennies, la recherche a révélé l’importance de cet écosystème dans de nombreux aspects de la santé humaine, y compris la digestion, l’immunité et même la santé mentale. Plus récemment, les scientifiques ont commencé à explorer le lien entre le microbiote intestinal et le cancer, ouvrant ainsi de nouvelles perspectives pour la prévention et le traitement de cette maladie redoutée.
Comprendre le Microbiote
Le microbiote intestinal est composé de trillions de bactéries, virus, champignons et autres micro-organismes. Ces habitants de notre intestin jouent un rôle crucial dans la digestion des aliments, la production de vitamines et la protection contre les pathogènes. Un équilibre sain du microbiote est essentiel pour le bon fonctionnement de notre système immunitaire.
Microbiote et Cancer : Le Lien
Les recherches suggèrent que le microbiote peut influencer le développement et la progression du cancer de plusieurs manières :
1. **Inflammation Chronique** : Un déséquilibre du microbiote, appelé dysbiose, peut entraîner une inflammation chronique de l’intestin. Cette inflammation persistante peut endommager l’ADN des cellules et favoriser la transformation de cellules normales en cellules cancéreuses.
- 2. **Modulation du Système Immunitaire** : Le microbiote joue un rôle essentiel dans la régulation du système immunitaire. Un microbiote déséquilibré peut affaiblir la réponse immunitaire, rendant l’organisme moins capable de détecter et de détruire les cellules cancéreuses.
3. **Métabolites Bactériens** : Les bactéries intestinales produisent divers métabolites, dont certains peuvent avoir des effets protecteurs contre le cancer, tandis que d’autres peuvent être cancérigènes. Par exemple, certains acides gras à chaîne courte produits par des bactéries bénéfiques peuvent avoir des propriétés anticancéreuses.
#### Études Clés et Découvertes
De nombreuses études ont exploré le rôle du microbiote dans différents types de cancer. Par exemple :
– **Cancer Colorectal** : Les chercheurs ont trouvé des différences significatives dans la composition du microbiote intestinal entre les personnes atteintes de cancer colorectal et les individus en bonne santé. Certaines bactéries, comme Fusobacterium nucleatum, sont associées à une progression plus rapide de la maladie.
– **Cancer du Sein** : Des études préliminaires suggèrent que le microbiote intestinal pourrait influencer le risque de cancer du sein en modulant les niveaux d’œstrogènes circulants.
– **Immunothérapie et Cancer** : Il a été démontré que la composition du microbiote intestinal peut affecter la réponse aux traitements d’immunothérapie chez les patients atteints de cancer. Un microbiote diversifié et équilibré semble améliorer l’efficacité de ces traitements.
#### Perspectives pour la Prévention et le Traitement
L’étude du lien entre le microbiote et le cancer ouvre des avenues prometteuses pour de nouvelles approches thérapeutiques. Par exemple :
– **Probiotiques et Prébiotiques** : L’utilisation de probiotiques (bactéries bénéfiques) et de prébiotiques (fibres alimentaires favorisant la croissance des bonnes bactéries) pourrait aider à maintenir un microbiote sain et potentiellement réduire le risque de certains cancers.
– **Transplantation de Microbiote Fécal** : Cette technique, qui consiste à transférer le microbiote d’un donneur sain à un patient, est déjà utilisée pour traiter certaines infections intestinales récalcitrantes et est explorée comme une option pour moduler le microbiote chez les patients atteints de cancer.
– **Nutrition Personnalisée** : Adapter l’alimentation pour favoriser un microbiote équilibré pourrait devenir une stratégie clé dans la prévention du cancer.
#### Conclusion
Le lien entre le microbiote et le cancer est un domaine de recherche en plein essor qui promet de transformer notre compréhension et notre approche du cancer. Bien que beaucoup reste à découvrir, les preuves actuelles suggèrent que maintenir un microbiote intestinal sain pourrait jouer un rôle crucial dans la prévention et le traitement de cette maladie complexe. Investir dans la recherche sur le microbiote pourrait ainsi ouvrir de nouvelles voies pour améliorer la santé publique et offrir des espoirs tangibles aux patients atteints de cancer.

par admin | Juil 10, 2024 | Santé
 Le sulforaphane, un composé naturellement présent dans les germes de brocoli, suscite un intérêt croissant dans le domaine de la recherche sur le cancer en raison de ses propriétés anticancéreuses prometteuses.
Le sulforaphane, un composé naturellement présent dans les germes de brocoli, suscite un intérêt croissant dans le domaine de la recherche sur le cancer en raison de ses propriétés anticancéreuses prometteuses.
Des études ont montré que le sulforaphane peut aider à prévenir la croissance des cellules cancéreuses, à induire l’apoptose (mort cellulaire programmée) des cellules cancéreuses, et à inhiber la formation de vaisseaux sanguins qui alimentent les tumeurs.
Les germes de brocoli sont une excellente source de sulforaphane, car ils contiennent une concentration élevée de cette substance bénéfique. En incorporant les germes de brocoli dans votre alimentation, vous pouvez potentiellement bénéficier de leurs effets anticancéreux.
Il est important de noter que bien que le sulforaphane montre un grand potentiel dans la lutte contre le cancer, il ne doit pas être considéré comme un traitement unique. Il est essentiel de consulter un professionnel de la santé pour obtenir un plan de traitement approprié en cas de diagnostic de cancer.
En conclusion, le sulforaphane présent dans les germes de brocoli offre un espoir dans la recherche de nouvelles approches pour le traitement du cancer. En intégrant ces aliments riches en sulforaphane dans une alimentation équilibrée, il est possible de bénéficier de leurs propriétés anticancéreuses potentielles.
N’oubliez pas de consulter un professionnel de la santé pour toute question concernant le traitement du cancer ou l’intégration de nouveaux aliments dans votre alimentation.

par admin | Juil 10, 2024 | Santé
Tout ce que David Sinclair mange – et évite – pour inverser le vieillissement
David Sinclair est un biologiste et universitaire australo-américain connu pour ses recherches sur le vieillissement et l’épigénétique. Sinclair est professeur de génétique à la Harvard Medical School et codirecteur du Paul F. Glenn Center for Biology of Aging Research. Il a été président de l’Académie de recherche sur la santé et la durée de vie.
Tout est dans l’assiette, la supplémentation, le sport et manger moins souvent (pas moins, mais en respectant une durée de jeûne dans la journée).
David a 54 ans, mais les résultats de son test d’âge biologique affirment qu’il n’a que 42 ans.
Voici ce que David Sinclair mange pour optimiser ses gènes pour une vie plus saine et plus longue.
Mangez pour vos gènes
« Une partie du problème avec le vieillissement est que vous commencez à avoir ce déroulement de l’ADN, et que des gènes qui ne devraient pas être activés le sont », explique Sinclair. Comment et quand vous mangez devrait viser à corriger le cours de ces gènes rebelles, selon Sinclair. Plus précisément, trois gènes : mTOR, AMPK et les sirtuines. Voici un cours accéléré rapide.
Activer les sirtuines
Les sirtuines sont une famille de gènes de longévité. « Il a été démontré que cette famille est un régulateur central très important de la longévité », explique Sinclair. Des études ont montré que les sirtuines jouent un rôle clé dans la réponse cellulaire à divers facteurs de stress, tels que le stress oxydatif ou génotoxique, et sont cruciales pour le métabolisme cellulaire (1).
Vous vous souvenez peut-être des sirtuines issues de recherches tristement célèbres qui ont émergé du laboratoire de Sinclair au début des années 2000, et qui ont révélé que le vin rouge pourrait en fait être bon pour vous. La recherche a découvert que le polyphénol resvératrol, présent dans le vin rouge, active la sirtuine SIRT-1 (2).
Il est intéressant de noter que les sirtuines sont activées par le stress. « Le jeûne active les sirtuines, l’exercice active les sirtuines – les choses génériques que les médecins nous disent de faire, nous pensons qu’elles sont médiées par les sirtuines », explique Sinclair.
Supprimer mTOR
Lorsque vous mangez des protéines, le gène de la rapamycine (mTOR) cible chez les mammifères est activé. mTOR est responsable de la régulation de la production de protéines et influence directement la croissance, la division et la survie des cellules.
« Lorsque vous mangez un gros steak, mTor est activé », explique Sinclair. « Et c’est pourquoi vous développez plus de muscle que si vous ne mangez pas beaucoup de protéines. »
Génial, n’est-ce pas ? Non. Un certain degré de masse musculaire est important pour la longévité (3), et Sinclair précise que nous avons besoin de protéines pour prospérer ; cependant, trop de mTOR est lié à des maladies liées à l’âge comme le diabète et le cancer (4, 5).
« Si vous régulez à la baisse l’activité de ce complexe protéique mTOR, vous obtenez une durée de vie plus longue », explique Sinclair, « parce qu’il active un processus appelé autophagie, qui recycle les protéines. » Un processus qui améliore les performances cellulaires, vous gardant en bonne santé.
Activer l’AMPK
La protéine kinase activée par l’adénosine 5′ monophosphate (AMPK) est une enzyme connue comme le principal régulateur du métabolisme énergétique de l’organisme.
« L’une des principales choses que [l’AMPK] fait, c’est qu’il produit plus de mitochondries. Nous perdons des mitochondries à mesure que nous vieillissons », explique Sinclair. Une mauvaise fonction mitochondriale est liée aux maladies cardiaques (6), à la démence (7), au diabète de type 2 (8), au syndrome métabolique (9) et à la résistance à l’insuline (10).
« Les mitochondries sont importantes pour métaboliser ce que nous mangeons et produire de l’énergie chimique », explique Sinclair. « C’est pourquoi, lorsque vous activez l’AMPK, vous avez plus d’énergie et vous vous sentez mieux. »
« L’AMPK joue également un rôle central de régulateur des défenses de l’organisme », explique Sinclair. « Il régulera à la baisse mTOR et activera d’autres gènes de longévité. Ces gènes travaillent de concert les uns avec les autres.
L’AMPK est liée à la glycémie. Lorsque les cellules sont privées de glucose, comme lors du jeûne, l’AMPK est activée. Cela peut être reproduit avec la metformine, un médicament utilisé pour traiter le diabète de type 2 qui peut abaisser les niveaux de glucose dans le corps, améliorer la sensibilité à l’insuline et réduire les symptômes du vieillissement (11). C’est exactement pourquoi la metformine est le sujet vedette des essais cliniques en cours sur l’anti-âge (12, 13).
Quand manger
Selon Sinclair, manger moins souvent peut aider à optimiser vos gènes. « Il ne s’agit pas seulement de la période de repas, c’est la période de non-alimentation qui est si importante pour renforcer les défenses de l’organisme contre le vieillissement afin de maximiser la longévité », dit-il.
Pourquoi? Le stress dû au jeûne déclenche un changement métabolique optimal dans vos gènes, en régulant à la hausse les sirtuines et l’AMPK, et en régulant à la baisse mTOR. Le jeûne est associé à de meilleurs résultats pour les personnes atteintes du syndrome métabolique (14), du prédiabète (15), du diabète (16), de la sclérose en plaques (17) et du cancer du sein (18).
Selon Sinclair, il n’y a pas qu’une seule bonne façon de jeûner. « Vous êtes un individu, vous avez un mode de vie différent, une tolérance à la douleur et à la faim, et le microbiome – ce sont des choses vraiment importantes à prendre en considération », dit-il. Il recommande d’essayer l’une des trois méthodes de jeûne ci-dessous.
Jeûne prolongé
Le jeûne prolongé est une période de plus d’une journée – les gens vont un jour, trois jours, et d’autres, une semaine.
« Ces périodes prolongées vont faire un véritable nettoyage en profondeur du corps et activer cette autophagie. Surtout une fois que vous avez passé la barre des trois jours, lorsque votre métabolisme passe à ce qu’on appelle l’autophagie médiée par le chaperon (20), également connue sous le nom de nettoyage en profondeur », explique-t-il.
Alimentation limitée dans le temps
Le plus pratique des protocoles de jeûne suggérés par Sinclair, et celui qu’il suit, consiste à manger pendant un bloc de temps spécifique de la journée et à jeûner pour le reste. Les protocoles d’alimentation populaires limités dans le temps comprennent le jeûne intermittent 18 :6 – où vous jeûnez pendant 18 heures et mangez pendant 6 heures – et 20 :4 – où vous jeûnez pendant 20 heures et mangez pendant 4 heures.
« Vous voulez avoir au moins 16 heures sans manger ou pas beaucoup », explique Sinclair. « Donc, généralement, cela signifie prendre un déjeuner tardif si vous sautez le petit-déjeuner, ou si vous préférez sauter le dîner, vous pouvez sauter cela. »
Lorsque vous jeûnez, votre foie compense le manque de nourriture en déclenchant la gluconéogenèse, un processus par lequel le foie transforme le lactate, les acides aminés et le glycérol en glucose pour produire de l’énergie. Après plusieurs semaines de jeûne intermittent régulier, votre foie commencera à produire du glucose à un niveau stable, évitant efficacement la hausse et la baisse du glucose qui se produisent lorsque vous mangez des repas réguliers tout au long de la journée.
Régime imitant le jeûne
Le « régime imitant le jeûne » a été développé par Valter Longo, un chercheur de l’UCLA. Ses travaux ont révélé qu’un régime imitant le jeûne aidait les patients atteints de cancer à survivre et à surmonter la chimiothérapie plus rapidement (19).
Le régime est parfait pour les personnes qui veulent profiter des bienfaits du jeûne mais qui ne veulent pas renoncer complètement à la nourriture. Il s’agit de restreindre sévèrement vos calories (à 1 100 calories par jour) pendant cinq jours par mois. Au cours de laquelle, vous vous concentrez sur la consommation d’aliments entiers à base de plantes, faibles en glucides et en protéines, et riches en graisses saines.
Ce profil nutritionnel spécifique (lorsqu’il est délivré en quantités précises) imite la réponse physiologique de votre corps au jeûne traditionnel. Selon Sinclair, la sauce secrète consiste à manger moins de viande, ce qui supprime mTOR.
Pour suivre le régime, préparez des recettes de longévité directement dans la cuisine de Longo ou essayez ProLon, un service développé par Longo pour que tout ce dont vous avez besoin pour suivre un régime de jeûne imitant cinq jours soit livré directement à votre porte une fois par mois.
La méthode de jeûne intermitent selon Sinclair
Sinclair affirme que sa pratique du jeûne l’a aidé à perdre 15 livres et à retrouver son corps de vingt ans, ce qu’il considère comme un bonus supplémentaire aux avantages de la longévité.
- Il suit un programme de jeûne 20 :4 où il essaie de ne pas manger avant le dîner, puis prend un « grand dîner vraiment agréable ».
- Il boit beaucoup d’eau tout au long de la journée, ce qui aide à réduire sa sensation de faim, et lorsqu’il a absolument besoin de grignoter quelque chose, il prend une petite poignée de noix.
- Il mélange un peu de yaourt avec ses suppléments pour les dissoudre. L’association de vitamines liposolubles (A, D, E et K) avec des graisses peut aider à l’absorption.
- Il boit Athletic Greens le matin pour compenser certains des nutriments potentiellement manqués par le jeûne qui peuvent l’aider à fonctionner plus tôt dans la journée.
Ce qu’il faut manger
Le jeûne concerne généralement plus le moment où vous mangez que ce que vous mangez. Cependant, le jeûne, en particulier lorsqu’il est pratiqué pour la longévité, fonctionne mieux avec une alimentation saine, selon Sinclair. « Une nutrition adéquate est nécessaire, sinon vous ferez plus de mal que de bien à votre corps », explique Sinclair.
Qu’est-ce que cela implique exactement ? Pour Sinclair, l’accent est mis sur la consommation d’un seul type d’aliment pour vivre plus longtemps : les plantes.
Plus de plantes
Selon Sinclair, plus vous mangez de plantes, mieux c’est. Il recommande spécifiquement de se concentrer sur les aliments végétaux contenant des polyphénols comme les baies, le vin rouge, le matcha, les olives (et l’huile d’olive), les haricots et les légumes comme les artichauts, la chicorée, l’oignon rouge et les épinards.
Pourquoi? Les polyphénols, comme le resvératrol, le piceatannol, la fisétine et la quercétine activent les sirtuines.
Il est intéressant de noter que plus vous stressez une plante, plus elle produit de polyphénols pour l’aider à survivre. C’est pourquoi les aliments qui sont intentionnellement stressés, comme le vin rouge, sont riches en polyphénols. « Les meilleurs vins rouges sont ceux où les vignes sont déshydratées ou où poussent des champignons. Il y a une bonne raison à cela », explique M. Sinclair. (Conseil de pro : si vous êtes un amateur de vin, choisissez le pinot noir – selon Sinclair, c’est le plus riche en resvératrol, le polyphénol actif).
Le record : dans notre approvisionnement alimentaire, nos plantes ne subissent pas beaucoup de stress. M. Sinclair explique que les plantes cultivées plus grandes et plus rapidement sont plus rentables pour les agriculteurs. mais, ne sont pas susceptibles de contenir des polyphénols.
Comment savoir si votre alimentation est stressée ? « Eh bien, vous pouvez commencer par la généralisation selon laquelle s’ils sont cultivés dans un champ de manière biologique, sans pesticides, ils sont probablement plus stressés », explique Sinclair. « Ce que je recherche, ce sont des plantes biologiques, locales et colorées, car ce sont les plus susceptibles d’être riches en ces molécules. »
Ce qu’il ne faut pas manger
La liste des aliments à ne pas manger de Sinclair est légèrement plus longue. Cependant, il est clair que votre régime alimentaire ne doit pas être restrictif et inclure des quantités adéquates de macronutriments pour alimenter votre corps pour la vie (et il admet rapidement qu’il mange sa juste part de dessert). Cependant, ces deux aliments peuvent faire des ravages sur vos gènes lorsqu’ils sont consommés en excès. Voici le scoop.
Sucre
À un niveau élevé, le glucose désactive les mécanismes de protection de votre corps, l’AMPK et les sirtuines. Pour éviter ce changement défavorable, Sinclair recommande de manger moins de sucre et de viser à maintenir des niveaux de glucose constants.
« Si vous mangez trois repas par jour plus des collations, votre glycémie augmentera et vos défenses contre le vieillissement fonctionneront au minimum », explique Sinclair. Il recommande de surveiller les niveaux de glucose à l’aide d’un glucomètre en continu et d’ajuster votre alimentation en conséquence pour minimiser les pics.
Viande
« Il est certain que si vous êtes un athlète ou si vous voulez prendre du volume, il y a des gains à court terme à manger de la viande », dit-il. « Vous vous sentirez mieux si vous mangez de la viande, vous aurez les protéines pour développer ce muscle. » Dans ces cas, vous avez besoin de plus de protéines pour maintenir des niveaux élevés d’activité, et l’activation de mTOR joue un rôle important dans la construction musculaire.
Bien que ce soit une bonne chose à court terme, selon Sinclair, « mTOR peut faire quelque chose d’encore mieux pour la longévité à long terme en étant régulé à la baisse et en activant l’autophagie ». Il note que mTOR peut parfois être activé, mais que vous ne voulez pas qu’il soit activé tout le temps.
En donnant à votre corps une pause périodique dans le traitement des acides aminés, en particulier les BCAA (leucine, isoleucine et valine) qui activent mTOR, vous donnerez à votre corps une chance de puiser dans l’autophagie. Cela ne signifie pas que vous devez renoncer à la viande, Sinclair suggère que le jeûne intermittent est suffisant pour réguler à la baisse mTOR.
Mangez comme Sinclair
Sinclair se concentre sur un régime méditerranéen rempli de fruits et de légumes. Voici comment il le décompose.
- Il ne mange pas de viande, choisissant d’obtenir ses protéines à partir de sources végétales.
- Il achète des fruits et légumes biologiques, locaux et colorés qui sont les plus susceptibles d’être remplis de polyphénols.
- Il cuisine avec de l’huile d’olive pour activer les sirtuines.
- Il évite le sucre et s’appuie sur des alternatives sans sucre pour ajouter de la douceur à sa nourriture.
- S’il mange du sucre, il le mange à la fin du repas pour réduire les pics de glucose.






 Le glaucome est une maladie oculaire caractérisée par des dommages progressifs au nerf optique, souvent associés à une pression intraoculaire élevée. Il existe plusieurs types de glaucome, mais le plus courant est le glaucome à angle ouvert. Si elle n’est pas traitée, cette condition peut entraîner une perte de vision irréversible.
Le glaucome est une maladie oculaire caractérisée par des dommages progressifs au nerf optique, souvent associés à une pression intraoculaire élevée. Il existe plusieurs types de glaucome, mais le plus courant est le glaucome à angle ouvert. Si elle n’est pas traitée, cette condition peut entraîner une perte de vision irréversible.


 L’huile d’olive, un pilier de la cuisine méditerranéenne, est bien connue pour ses nombreux bienfaits pour la santé, notamment ses effets anti-inflammatoires et cardioprotecteurs. Cependant, une facette moins explorée de cette huile précieuse est son influence sur le microbiote intestinal. Dans cet article, nous allons plonger dans les effets de l’huile d’olive sur notre microbiote et comprendre pourquoi cette alliance est bénéfique pour notre santé globale.
L’huile d’olive, un pilier de la cuisine méditerranéenne, est bien connue pour ses nombreux bienfaits pour la santé, notamment ses effets anti-inflammatoires et cardioprotecteurs. Cependant, une facette moins explorée de cette huile précieuse est son influence sur le microbiote intestinal. Dans cet article, nous allons plonger dans les effets de l’huile d’olive sur notre microbiote et comprendre pourquoi cette alliance est bénéfique pour notre santé globale. 1. Effet Prébiotique : Les polyphénols de l’huile d’olive peuvent agir comme des prébiotiques, c’est-à-dire qu’ils favorisent la croissance des bactéries bénéfiques dans l’intestin. Ces composés sont métabolisés par les bactéries intestinales, produisant ainsi des métabolites bénéfiques comme les acides gras à chaîne courte (AGCC), qui sont essentiels pour la santé intestinale et globale.
1. Effet Prébiotique : Les polyphénols de l’huile d’olive peuvent agir comme des prébiotiques, c’est-à-dire qu’ils favorisent la croissance des bactéries bénéfiques dans l’intestin. Ces composés sont métabolisés par les bactéries intestinales, produisant ainsi des métabolites bénéfiques comme les acides gras à chaîne courte (AGCC), qui sont essentiels pour la santé intestinale et globale. 1. Utilisation Quotidienne : Utilisez l’huile d’olive comme principal corps gras pour la cuisson et l’assaisonnement. Elle est idéale pour les salades, les légumes rôtis et les marinades.
1. Utilisation Quotidienne : Utilisez l’huile d’olive comme principal corps gras pour la cuisson et l’assaisonnement. Elle est idéale pour les salades, les légumes rôtis et les marinades.

 Le sulforaphane, un composé naturellement présent dans les germes de brocoli, suscite un intérêt croissant dans le domaine de la recherche sur le cancer en raison de ses propriétés anticancéreuses prometteuses.
Le sulforaphane, un composé naturellement présent dans les germes de brocoli, suscite un intérêt croissant dans le domaine de la recherche sur le cancer en raison de ses propriétés anticancéreuses prometteuses.